Nowości z przeszłości
O świecie z punktów złożonym
Jednym z najbardziej fundamentalnych zadań poznawczych fizyki jest odpowiedź na pytania dotyczące struktury materii: Z czego zbudowane są różne ciała materialne: gazy, ciecze, ciała stałe, planety, Słońce, gwiazdy? Czy oszałamiająca różnorodność otaczającego nas świata materialnego nie jest tylko wynikiem składania (mieszania) pewnej niewielkiej liczby podstawowych elementów branych w różnych proporcjach? Jeśli tak, to ile jest tych elementów i jakie są ich własności?

Pytania te postawili 25 wieków temu greccy filozofowie przyrody. Jednakże podane przez nich próby odpowiedzi były oparte na powierzchownych obserwacjach przyrody i miały charakter czysto racjonalnych, spekulatywnych rozważań, nie poddanych żadnym bardziej wnikliwym testom eksperymentalnym. Fizyka nowożytna, której początek datuje się na przełom XVI i XVII w., przez pierwsze dwa wieki swego istnienia nie zajmowała się zagadnieniem elementarnych składników materii. Fizycy koncentrowali się w tym okresie na rozwijaniu ilościowej racjonalno-empirycznej metody naukowej (przejętej później przez całe przyrodoznawstwo) i na niezwykle owocnym stosowaniu tej nowej metody do badania makroskopowych zjawisk mechanicznych, termicznych, optycznych, elektrycznych i magnetycznych. Problemem elementów zajmowali się natomiast chemicy, ale również od strony czysto makroskopowej, starając się zdefiniować i wyodrębnić pewne podstawowe substancje zwane pierwiastkami chemicznymi.
Z drugiej strony, fizycy już w XVIII w., a nawet jeszcze w wieku XVII, wskazywali na możliwość wytłumaczenia niektórych zjawisk makroskopowych (np. optycznych, termicznych itd.) za pomocą pewnych mikroskopowych korpuskularnych modeli podobnych do atomistycznych modeli Demokryta z IV w. p.n.e. Były to jednak rozważania zupełnie niezwiązane z poszukiwaniami pierwiastków chemicznych. Zbliżenie tych dwóch kierunków poszukiwań nastąpiło dopiero na początku XIX w., wkrótce po odkryciu przez chemików podstawowych praw stechiometrii: prawa stosunków stałych, prawa stosunków wielokrotnych i prawa stosunków równoważnikowych. Dopóki traktowano pierwiastki i związki chemiczne w sposób czysto makroskopowy jako ciągłe jednorodne substancje, wymienione prawa stechiometrii były zupełnie niezrozumiałe i zaskakujące. W 1808 r. J. Dalton podał bardzo proste i poglądowe wyjaśnienie tych praw za pomocą hipotezy molekularno-atomowej. Hipoteza Daltona stanowiła wymagane przez fakty doświadczalne pogłębienie starego atomistycznego modelu mikroskopowej struktury materii Demokryta i tym samym przeniosła problem elementarnych składników materii z poziomu makroskopowego na poziom mikroskopowy. Według tej hipotezy wszystkie ńormalnećiała materialne mają strukturę nieciągłą i składają się z dyskretnych ziarenek materii o określonych masach, zwanych molekułami. Molekuły chemiczne czystego ciała są jednakowe i są zbudowane w ściśle określony sposób z jeszcze bardziej elementarnych ziarenek, zwanych atomami, odpowiadających pierwiastkom chemicznym. Molekuły mogą zawierać więc tylko określoną liczbę naturalną 0, 1, 2,... atomów każdego pierwiastka. Widać od razu, że ze stosunkowo niewielkiej liczby kilkudziesięciu pierwiastków można złożyć ogromną (właściwie nieskończoną) liczbę molekuł. Atomy miały być według Daltona niepodzielne i niezniszczalne, a wszelkie reakcje chemiczne miały polegać na ich łączeniu w molekuły, tudzież na przegrupowaniach atomów, podziałach molekuł itp.
Dalton założył jednak mylnie, że molekuły pierwiastków chemicznych są zawsze jednoatomowe, co spowodowało dużo zamieszania i opóźniło przyjęcie hipotezy Daltona przez ogół chemików o ponad 50 lat. Wprawdzie już w 1811 r. fizyk Avogadro wysunął przypuszczenie, że molekuły wielu gazowych pierwiastków (np. tlenu, azotu, chloru itd.) są dwuatomowe, ale chemicy jakoś zignorowali to proste rozwiązanie trudności.
Około połowy XIX w. hipoteza molekularno-atomowej struktury materii stała się jednym z głównych przedmiotów teoretycznych badań fizyków. Było to związane głównie ze sformułowaniem w tym okresie dwóch podstawowych zasad termodynamiki. Zasady te podają pewne bardzo ogólne związki między procesami mechanicznymi, termicznymi i chemicznymi zachodzącymi w dowolnych ciałach makroskopowych. Niestety, termodynamika nie dawała możliwości obliczenia oraz głębszej interpretacji licznych wielkości występujących w jej równaniach, jak np. równania stanu, energii wewnętrznej, entropii, temperatury itd., podając tylko pewne związki między tymi wielkościami. Fizycy dojrzeli więc w mikroskopowych modelach możliwość pogłębienia i uzupełnienia makroskopowej termodynamiki. Pierwsza ilościowa teoria mikroskopowa, zwana teorią kinetyczną gazów, opierała się na bardzo prostych i poglądowych mechanistycznych założeniach modelowych. Przyjmowało się w niej, że chemicznie czysty gaz składa się z jednakowych molekuł o określonej masie, poruszających się bezładnym ruchem i mogących się zderzać elastycznie ze sobą oraz ze ściankami naczynia.
W pierwszym przybliżeniu zakłada się, że molekuły są punktami materialnymi; w następnym zakłada się, że są one sztywnymi kulkami o ustalonym promieniu, które mogą się zderzać elastycznie. Następnie uwzględnia się centralne siły krótkiego zasięgu między kulkami. W bardziej pogłębionych modelach uwzględnia się częściowo strukturę atomową molekuł, wyrażającą się m.in. w odstępstwie od kulistej symetrii, występowaniu rotacji dokoła środka masy molekuł itd. Już te najprostsze modele gazu pozwalają na głębsze zrozumienie fizycznego sensu temperatury, ciśnienia, entropii, energii wewnętrznej itd., na wyprowadzenie i mikroskopową interpretację równań termodynamiki oraz na obliczenie różnych funkcji termodynamicznych, jak np. równania stanu, ciepła właściwego, entropii itd.
Badania roztworów elektrolitów, a później badania wyładowań w rozrzedzonych gazach doprowadziły w drugiej połowie XIX w. do odkrycia elektronu i ziarnistości ładunku elektrycznego, który poprzednio był uważany za ciągłą substancję. Okazało się, że ładunki elektryczne występujące w przyrodzie są zawsze całkowitymi wielokrotnościami pewnego elementarnego ładunku e, równego co do wielkości ładunkowi elektronu. Po sformułowaniu przez Maxwella w latach 70-tych makroskopowej, fenomenologicznej elektrodynamiki powstało zapotrzebowanie na jej mikroskopowe pogłębienie. Zapoczątkował ten proces Lorentz, formułując podstawy teorii elektronowej, opartej na założeniu istnienia elektronów, które mogą być swobodne lub związane, zależnie od rodzaju ciała.
Odkrycie istnienia jonów i elektronów oznaczało, że - wbrew pierwotnym założeniom Daltona i innych badaczy - elektrycznie neutralne atomy nie są niepodzielne. Wydawało się jednak, że oddzielanie lub przyłączanie elektronów przez molekuły i atomy nie narusza chemicznej integralności tych ostatnich, wyrażonej przez prawo zachowania całkowitej liczby atomów każdego pierwiastka z osobna. Dopiero odkrycie naturalnej promieniotwórczości w końcu XIX w. dowiodło, że atomy nie są ani niepodzielne, ani niezniszczalne. Już w XX w. odkryto, że atomy pierwiastka o liczbie porządkowej 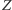 składają się ze stosunkowo ciężkiego jądra o dodatnim ładunku
składają się ze stosunkowo ciężkiego jądra o dodatnim ładunku 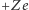 i o wymiarach
i o wymiarach 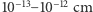 oraz krążących wokół niego na odległościach rzędu
oraz krążących wokół niego na odległościach rzędu 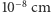
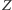 elektronów, z których każdy niesie ujemny ładunek elementarny
elektronów, z których każdy niesie ujemny ładunek elementarny 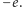 Teorią, opisującą bardzo dobrze wewnętrzną strukturę atomów, jonów i molekuł oraz ich wszystkie mechaniczne, elektryczne, magnetyczne, optyczne i chemiczne własności, jest powstała około 1925 r. mechanika kwantowa. W porównaniu z XIX-wiecznymi teoriami makroskopowymi został zmieniony bardzo poważnie aparat matematyczny, ale pozostały niezmienione podstawowe koncepcje modelowe, traktujące atom czy molekułę jak układ mechaniczny złożony z określonej liczby punktów materialnych, między którymi występują tylko znane siły elektromagnetyczne.
Teorią, opisującą bardzo dobrze wewnętrzną strukturę atomów, jonów i molekuł oraz ich wszystkie mechaniczne, elektryczne, magnetyczne, optyczne i chemiczne własności, jest powstała około 1925 r. mechanika kwantowa. W porównaniu z XIX-wiecznymi teoriami makroskopowymi został zmieniony bardzo poważnie aparat matematyczny, ale pozostały niezmienione podstawowe koncepcje modelowe, traktujące atom czy molekułę jak układ mechaniczny złożony z określonej liczby punktów materialnych, między którymi występują tylko znane siły elektromagnetyczne.
W 1932 r. odkryto neutron jako drugą obok protonu cząstkę składową jąder atomowych. Okazało się, że jądra tego samego pierwiastka mają zawsze tę samą liczbę 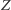 protonów, ale liczba neutronów może być różna (izotopy). Znajomość cząstek składowych jądra i ich podstawowych własności pozwoliła na przystąpienie do budowy teorii opisującej strukturę jądra i procesy zachodzące w reakcjach jądrowych. Podobnie jak w przypadku atomu traktuje się jądro jak mechaniczny układ złożony z
protonów, ale liczba neutronów może być różna (izotopy). Znajomość cząstek składowych jądra i ich podstawowych własności pozwoliła na przystąpienie do budowy teorii opisującej strukturę jądra i procesy zachodzące w reakcjach jądrowych. Podobnie jak w przypadku atomu traktuje się jądro jak mechaniczny układ złożony z 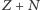 punktów oddziałujących wzajemnie odpowiednimi siłami krótkiego zasięgu, zwanymi siłami jądrowymi. Podstawę formalną teorii jądra stanowi mechanika kwantowa. Jednakże siły jądrowe nie mają makroskopowego odpowiednika i tym samym nie dają się zmierzyć bezpośrednio za pomocą jakichś cząstek próbnych. Jesteśmy więc zdani na wnioskowania pośrednie, które są bardzo skomplikowane i dają niejednoznaczne wyniki. Nic więc dziwnego, że nie znając dobrze sił jądrowych, teoria jądra jest jeszcze niezadowalająca i daleka od dokładności teorii atomu. Znaczna większość fizyków sądzi jednak, że jest to spowodowane tylko niedostateczną znajomością oddziaływań między nukleonami, a nie błędnością traktowania jądra jako układu punktów materialnych.
punktów oddziałujących wzajemnie odpowiednimi siłami krótkiego zasięgu, zwanymi siłami jądrowymi. Podstawę formalną teorii jądra stanowi mechanika kwantowa. Jednakże siły jądrowe nie mają makroskopowego odpowiednika i tym samym nie dają się zmierzyć bezpośrednio za pomocą jakichś cząstek próbnych. Jesteśmy więc zdani na wnioskowania pośrednie, które są bardzo skomplikowane i dają niejednoznaczne wyniki. Nic więc dziwnego, że nie znając dobrze sił jądrowych, teoria jądra jest jeszcze niezadowalająca i daleka od dokładności teorii atomu. Znaczna większość fizyków sądzi jednak, że jest to spowodowane tylko niedostateczną znajomością oddziaływań między nukleonami, a nie błędnością traktowania jądra jako układu punktów materialnych.
Przez pewien czas wydawało się, że protony, neutrony, elektrony oraz neutrina (wylatujące z jąder w rozpadach 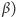 stanowią najmniejsze, niepodzielne i jedyne obok kwantów pola elektromagnetycznego - fotonów - składniki materii, które nazwano cząstkami elementarnymi. Zajęły one miejsce atomów, które okazały się podzielne i złożone. Trochę niepokojący był jednak fakt, że jedna z cząstek elementarnych, a mianowicie neutron, jest nietrwała, gdyż rozpada się w końcu na proton, elektron i neutrino. Jako cząstka składowa jądra neutron ma takie same silne oddziaływania jak proton i w jądrach stabilnych jest całkowicie trwały. Z drugiej strony, w niektórych jądrach niestabilnych właśnie proton rozpada się na neutron, pozyton (antyelektron) i neutrino. Zgodzono się więc, by włączyć nietrwały neutron do listy cząstek elementarnych. Niestety, około 1950 r. rozpoczęła się trwająca do dziś lawina odkryć coraz to nowych nietrwałych cząstek, które mimo nierzadko bardzo krótkiego czasu życia trzeba było z podobnych względów uznać za cząstki elementarne. Dzielą się one na silnie oddziałujące hadrony i z reguły lżejsze od nich słabo oddziałujące leptony, do których należy elektron i neutrino. Hadrony dzielą się z kolei na mezony o spinie całkowitym i bariony o spinie połówkowym. Proton i neutron należą do barionów. Hadronów znamy już bardzo dużo, bo ponad sto, i niemal co roku fizycy odkrywają nowe.
stanowią najmniejsze, niepodzielne i jedyne obok kwantów pola elektromagnetycznego - fotonów - składniki materii, które nazwano cząstkami elementarnymi. Zajęły one miejsce atomów, które okazały się podzielne i złożone. Trochę niepokojący był jednak fakt, że jedna z cząstek elementarnych, a mianowicie neutron, jest nietrwała, gdyż rozpada się w końcu na proton, elektron i neutrino. Jako cząstka składowa jądra neutron ma takie same silne oddziaływania jak proton i w jądrach stabilnych jest całkowicie trwały. Z drugiej strony, w niektórych jądrach niestabilnych właśnie proton rozpada się na neutron, pozyton (antyelektron) i neutrino. Zgodzono się więc, by włączyć nietrwały neutron do listy cząstek elementarnych. Niestety, około 1950 r. rozpoczęła się trwająca do dziś lawina odkryć coraz to nowych nietrwałych cząstek, które mimo nierzadko bardzo krótkiego czasu życia trzeba było z podobnych względów uznać za cząstki elementarne. Dzielą się one na silnie oddziałujące hadrony i z reguły lżejsze od nich słabo oddziałujące leptony, do których należy elektron i neutrino. Hadrony dzielą się z kolei na mezony o spinie całkowitym i bariony o spinie połówkowym. Proton i neutron należą do barionów. Hadronów znamy już bardzo dużo, bo ponad sto, i niemal co roku fizycy odkrywają nowe.
Okazało się jednak, że hadrony można pogrupować w pewne powtarzające się multiplety (np. oktety, dekuplety, singlety, nonety - patrz Delta 2/1979) charakteryzujące się tym, że występują w nich tylko określone kombinacje wartości ładunku oraz takich nowych liczb kwantowych, jak izospin, dziwność, powab itp. Występowanie powtarzających się multipletów przypomina trochę powtarzające się okresy pierwiastków chemicznych w tablicy Mendelejewa, które są związane ze strukturą powłok elektronowych atomu. Nic więc dziwnego, że w 1964 r. M. Gell-Mann i G. Zweig wysunęli hipotezę, że hadrony są obiektami złożonymi z jeszcze bardziej fundamentalnych (subelementarnych) cząstek, które nazwano kwarkami. Konwencjonalny model kwarkowy zakłada, że kwarki i antykwarki mają spin 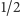 i ułamkowe ładunki elektryczne
i ułamkowe ładunki elektryczne 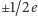 i
i 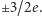 Mezony składają się z jednego kwarku i jednego antykwarku, a bariony z 3 kwarków. Nawet bez znajomości oddziaływań między kwarkami - stosując tylko argumenty symetrii oparte na mechanice kwantowej - można było nie tylko wytłumaczyć pochodzenie multipletów hadronowych, lecz także przewidzieć istnienie i własności licznych hadronów odkrytych później doświadczalnie.
Mezony składają się z jednego kwarku i jednego antykwarku, a bariony z 3 kwarków. Nawet bez znajomości oddziaływań między kwarkami - stosując tylko argumenty symetrii oparte na mechanice kwantowej - można było nie tylko wytłumaczyć pochodzenie multipletów hadronowych, lecz także przewidzieć istnienie i własności licznych hadronów odkrytych później doświadczalnie.

Korzystając z dotychczasowych doświadczeń historycznych i koncepcji, które już wielokrotnie sprawdziły się w przeszłości, fizycy przystąpili niezwłocznie do doświadczeń, zmierzających do rozbicia hadronów na pojedyncze kwarki, do wyodrębnienia pojedynczych kwarków i zbadania ich własności. I tu spotkała ich wielka niespodzianka. Wydawało się, że skoro z makroskopowego ciała można wydzielić jego cząstki składowe - molekuły, np. przez proste podgrzanie, skoro środkami chemicznymi lub fizycznymi można rozbić molekuły na atomy, skoro można rozbić - dostarczając odpowiedniej energii - atom na jądro i elektrony, a wreszcie jądro na protony i neutrony, to tak samo musi być możliwe rozbicie cząstek elementarnych na kwarki. Dotychczas do rozbicia każdego obiektu złożonego na cząstki składowe wystarczała energia dużo mniejsza od energii spoczynkowej tego obiektu. Tymczasem w zderzeniach między cząstkami elementarnymi, mimo użycia energii przekraczających wielokrotnie ich energie spoczynkowe, mimo szczegółowej analizy promieniowania kosmicznego, w którym występują energie o wiele rzędów wielkości wyższe od energii uzyskiwanych w laboratorium, nie odkryto dotychczas kwarków ani żadnych innych cząstek, które można by uważać za cząstki subelementarne. Wydaje się, że może tym razem naprawdę doszliśmy do kresu podzielności materii. Tak więc sytuacja jest bardzo ciekawa i zupełnie nowa pod wieloma względami. Liczne niewątpliwe sukcesy modelu kwarkowego utwierdzają przekonanie o realnym istnieniu kwarków, ale przekonanie to opiera się dotychczas tylko na dowodach pośrednich. Dowodu bezpośredniego w postaci izolowanych kwarków dotychczas nie ma.
Nie wiemy jeszcze, co to znaczy. Niektórzy fizycy próbują wytłumaczyć tę zagadkę, wprowadzając bardzo dziwne siły międzykwarkowe, które nie maleją ze wzrostem odległości, lecz pozostają stałe lub nawet rosną w miarę wzrostu odległości między kwarkami. Całkowite oddzielenie np. kwarku od antykwarku na nieskończoną odległość wymagałoby wtedy dostarczenia nieskończonej energii. Nie jest to prosta i przekonująca hipoteza, ale nie można jej też odrzucić.
Nie jest wykluczone, że rozwiązanie zagadki kwarków leży gdzie indziej, a mianowicie w nieprzydatności schematu pojęciowego mechaniki punktów do zagadnienia struktury cząstek elementarnych. Prawdą jest, że schemat ten był stosowany z powodzeniem na wielu kolejnych piętrach poznania przyrody, poczynając od opisu ruchu gwiazd, planet, rakiet, pocisków itd., aż do struktury ciał makroskopowych i kolejnych coraz mniejszych obiektów mikroskopowych: molekuł, jonów, atomów i jąder. W szczególności w dotychczasowych badaniach obiektów mikroświata udawało się zawsze wyjaśnić strukturę rozciągłego, zmiennego obiektu, przyjmując, że jest on złożony z pewnej liczby odpowiednio oddziałujących punktów masowych.
Trzeba jednak pamiętać, że pojęcie cząstki punktowej prowadzi zarówno w mechanice klasycznej, jak i kwantowej do różnych kłopotliwych nieciągłości i nieskończoności, które trzeba eliminować w sposób nader sztuczny. Pojęcie punktowej cząstki jest idealizacją matematyczną i dokładnie punktowych cząstek nie ma. Redukując za każdym razem problem struktury rozciągłego obiektu do mechaniki punktów, przyjmujemy z góry, że gmach poznania ma nieskończenie wiele pięter i nie ma w ogóle końca czy szczytu. Mówiąc konkretniej - w tej chwili interesują nas kwarki jako składniki hadronów. Za jakiś czas zaczniemy pytać, z jakich subkwarków składają się kwarki itd. w nieskończoność.
Może rzeczywiście jest to jedyna i najwłaściwsza droga poznania. Nie jest jednak wykluczone, że doszliśmy nie tylko do kresu podzielności materii, lecz także do kresu stosowalności standardowego, wielokrotnie powtarzanego schematu opartego na pojęciu punktu masowego i że trzeba będzie zastosować inne, adekwatniejsze pojęcia. Niektórzy fizycy idą w tym kierunku, wysuwając przypuszczenie, że kwarki należy uważać raczej za swoiste kwantowe oscylacje materii hadronowej, których nie można więc oddzielić od tej materii. Podobnie nie można oddzielić fali akustycznej od materialnego ośrodka, w którym się ona rozchodzi, i badać w próżni.
Podejmuje się więc próby modyfikacji i rozbudowy modelu kwarkowego, traktując kwarki nadal jak punkty masowe, lub też posługując się innymi analogiami, jak np. struny, oscylacji, kropli cieczy itd. Nie wiemy jeszcze, jak będzie wyglądało rozwiązanie zagadki cząstek elementarnych, ale warto zwrócić uwagę na to, że we wszystkich tych próbach opieramy się na takich czy innych analogiach zaczerpniętych z makroskopowej mechaniki. Może któraś z tych analogii okaże się trafna i płodna. Może się jednak okazać, że wszystkie te analogie zawiodą i okaże się, że nasz dotychczasowy zestaw analogii i schematów myślowych oraz opartych na nich pojęć jest po prostu za ubogi i nieadekwatny do opisu własności cząstek elementarnych.