Życie na żywo
W lustrzanym świecie cząsteczek
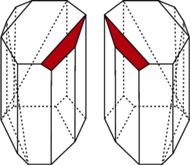
Badania kryształów otrzymanych z osadu pofermentacyjnego wina, prowadzone przez 26-letniego Ludwika Pasteura (1849), ujawniły istnienie ich dwu rodzajów, a Pasteur rozdzielił je pod mikroskopem igłą. Wykazywały lustrzaną symetrię, choć tworzył je ten sam związek, kwas winowy, którego cząsteczki mogły występować w dwu przestrzennych, lustrzanych formach. To była jedyna między nimi różnica. Roztwory rozseparowanych kryształów różnie skręcały spolaryzowane światło – w „prawo” (D) lub „lewo” (L). Takie cząsteczki często porównujemy do rękawiczek – jakkolwiek byśmy ich nie przekręcali, nie można nałożyć lewej rękawiczki na prawą rękę.
Dalsze badania ujawniły istnienie ogromnej liczby tego typu związków. Aby tworzyły się stereoizomery, wystarcza choć jeden tzw. asymetryczny atom węgla w cząsteczce (termin asymetryczny oznacza, że wiąże się on z czterema różnymi podstawnikami – omawiany kwas winowy ma dwa węgle asymetryczne).
Wikipedia
Kryształy...
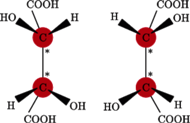
... i stereoizomery kwasu winowego (z lewej L, z prawej D).
Jeżeli prowadzić syntezę chemiczną związku mogącego tworzyć stereoizomery, powstaje po 50% każdego izomeru; taką mieszaninę nazywa się racematem, a proces przechodzenia jednej formy w drugą – racemizacją. Natomiast w żywych organizmach często występuje tylko jeden stereoizomer – klasycznym przykładem są białka, duże cząsteczki zbudowane z dwudziestu kilku aminokwasów, z których wszystkie (poza najmniejszym, glicyną), mogą tworzyć stereoizomery. Białka jednakże zbudowane są z L-aminokwasów, D-aminokwasy znajdujemy tylko pojedynczo w ścianach bakteryjnych i niektórych antybiotykach.
Dramatyczny przykład już ze współczesnych czasów to talidomid, lek, którego zażywanie przez ciężarne kobiety w USA, Niemczech, w latach 60. XX wieku wywoływało poważne zniekształcenia układu kostnego płodu. Talidomid uzyskiwany w syntezie chemicznej był racematem dwu form. Jedna z nich, jak się później okazało w badaniach na zwierzętach, powoduje zniekształcenia kończyn, druga – uśmierza ból. W kolejnych badaniach ustalono, że w lokalnych kwaśnych obszarach ludzkiego organizmu następuje racemizacja każdej z form, co ostatecznie wykluczyło talidomid z listy potencjalnych farmaceutyków stosowanych w czasie ciąży. Jak na ironię, talidomid jest użyteczny w leczeniu trądu i niektórych nowotworów.
Pytaniem oczywistym jest, dlaczego tylko L-aminokwasy budują białka, a D-aminokwasy dla nie-bakteryjnej komórki są wręcz truciznami. D-aminokwasy powstające po racemizacji rozkładającej się organicznej materii w glebie byłyby trujące dla roślin i zwierząt, gdyby nie trawiły ich bakterie. Wykazano to w laboratoryjnych i polowych doświadczeniach w różnych środowiskach, nawet pustynnych. W bakteriach do głosu dochodzi enzym, racemaza. O enzymie tym sądzi się, że pojawił się ewolucyjnie jako enzym odtruwający we wczesnym etapie życia na Ziemi. Racemizacji spontanicznej podlegają powoli wszystkie pozostałości organizmów po ich śmierci. Sądzono, że można by stosunek D/L form aminokwasów w paleobiologicznych próbkach użyć jako znacznika czasu, który upłynął od śmierci danego organizmu. Okazało się jednak, że prędkość racemizacji zależy od wielu czynników, z których najbardziej istotnym jest temperatura. Jej wysokość w historii znaleziska nie może być wiarygodnie oceniona – i tak pomysł ten zarzucono.
Najciekawszym, być może, pytaniem jest to, dlaczego tylko L-aminokwasy zostały użyte przez żywe organizmy we wczesnym okresie powstawania życia na Ziemi. W meteorytach przybyłych z Kosmosu znajdowane są i L- i D-aminokwasy w formie racematu. A gdyby tak stworzyć świat w odmiennej stereoformie?