Życie na żywo
Ze śmiertelnego zimna...
Bardzo znana anegdota głosi, że Fleming (bałaganiarz) nie umył płytek z zakończonym mikrobiologicznym doświadczeniem i po kilku dniach zauważył, że tam, gdzie na płytce w okolicy badanych przez niego stafilokoków pojawiło się zanieczyszczenie grzybem, tam stafilokoki zaczęły wymierać...
Po bliższym zbadaniu zjawiska (Fleming może nie od razu sprzątał po sobie, ale nie zostawiał niewyjaśnionych spraw niewyjaśnionymi) okazało się, że zabijała bakterie nieznana uprzednio substancja, wydzielana przez zanieczyszczającego grzyba, później zidentyfikowanego jako Penicillium notatum. Tak to podobno odkryto pierwszy antybiotyk – penicylinę. Od 60 lat przemysł produkujący różne antybiotyki rozwinął się niesłychanie, choć odkrywcom życie skomplikowały cechy bakterii i ewolucja: wśród miliardów bakterii zabijanych przez dany antybiotyk zawsze znajdzie się taki dziwoląg (genetycy mówią mutant), który jest na ten antybiotyk niewrażliwy, mutant mnoży się i mnoży, a jego wrażliwi „rodzice” giną i w końcu konkretny antybiotyk staje się w leczeniu konkretnej choroby bezużyteczny.
Po odkryciu Fleminga wielu starych ludzi przypomniało sobie o leczniczym działaniu pleśni przykładanej na rany, a uczeni o tym, że pleśni – według zapisów – używali starożytni Grecy i Hindusi do leczenia zakażeń.
Zjawisko rozpowszechniania się oporności na antybiotyki wśród szczepów szpitalnych odkryli po II wojnie światowej badacze japońscy, którzy bez umiaru stosowali antybiotyki i coraz częściej przekonywali się o zaniku ich aktywności. Przenoszenie się jednego genu oporności nie byłoby jeszcze takim nieszczęściem, lecz staje się nim pojawienie się zespołów genów oporności przeciw kilku różnym antybiotykom, przenoszonych jednocześnie. Stąd szczepy bakterii (gronkowiec złocisty), których nie zwalcza żaden znany antybiotyk.
Transfer genów między bakteriami warunkowany jest istnieniem bardzo szczególnych mechanizmów, częstych wśród bakterii i wirusów, usilnie poszukuje się ich w organizmach wyższych. Obszar badań tzw. horyzontalnego przekazywania genów, który odkryliśmy nie tak dawno, dziś spędza sen z oczu badaczy ewolucji świata mikroorganizmów. W tym świecie główną przyczyną ewolucji nie są powolne mutacje genów, lecz przenoszenie się genów. Ewolucjonistom dzisiejszym coraz trudniej postulować, która bakteria jest ewolucyjnie starsza, a która młodsza.
Okazało się także, że zjawisko rosnącej liczby przykładów oporności na antybiotyki w medycynie wywołały warunki terapii, brak wiedzy o mechanizmach tych zjawisk zarówno wśród lekarzy jak i pacjentów. Natomiast oporność taka wśród bakterii glebowych i w zbiornikach wodnych jest normą! To nie dziwi – wszak wiele pierwotnie stosowanych antybiotyków wytwarzają mikroorganizmy, rośliny, bezkręgowce i wydzielają je do środowiska – czemu nie miałyby tam selekcjonować opornych na nie bakterii?
Za sensacyjne jednak należy uznać znalezienie przez kanadyjskich
mikrobiologów w próbkach wiecznej zmarzliny bakterii sprzed 30 000 lat,
a w nich genów oporności na kilka antybiotyków, takich jak kodujący
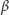 -laktamazę (oporność na penicylinę i jej pochodne laktamowe
antybiotyki), gen tetM chroniący przed tetracykliną i zespół trzech genów
nadających oporność na wankomycynę: vanH-vanA-vanX. Przy tak
starożytnym życiorysie nie mamy także pewności, czy i 30 tysięcy lat
temu geny te przeciwstawiały się antybiotykom, czy też miały inną,
nieznaną nam funkcję.
-laktamazę (oporność na penicylinę i jej pochodne laktamowe
antybiotyki), gen tetM chroniący przed tetracykliną i zespół trzech genów
nadających oporność na wankomycynę: vanH-vanA-vanX. Przy tak
starożytnym życiorysie nie mamy także pewności, czy i 30 tysięcy lat
temu geny te przeciwstawiały się antybiotykom, czy też miały inną,
nieznaną nam funkcję.