Aktualności (nie tylko) fizyczne
Zaskakujący metan
Metan ma kolosalne znaczenie. Jest nie tylko jednym z podstawowych paliw kopalnych, jednym z głównych gazów cieplarnianych, ale również jednym z najbardziej efektywnych mediów odnawialnych.
Chodzącymi źródłami metanu kiedyś były dinozaury, obecnie zastąpione przez np. krowy, ludzi czy termity. Samą produkcją zajmowały się i zajmują metanogeny (zaliczane do archeonów) zamieszkujące układy trawienne tych zwierząt oraz bagna, oczyszczalnie ścieków itp. Są beztlenowe, a metan jest produktem ich oddychania: 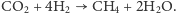 Reakcja ta jednak, jak wszystkie reakcje oddychania, nie zachodzi samoistnie, lecz jest katalizowana poprzez odpowiednie enzymy.
Reakcja ta jednak, jak wszystkie reakcje oddychania, nie zachodzi samoistnie, lecz jest katalizowana poprzez odpowiednie enzymy.

Końcowy etap łańcucha reakcji wygląda tak, że grupa metylowa 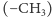 dostarczana jest przez metylo-koenzym M:
dostarczana jest przez metylo-koenzym M: 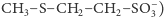 dokładnie w miejsce, gdzie we właściwym enzymie znajduje się atom niklu. Katalizuje on jej połączenie z ostatnim atomem wodoru (dostarczanym przez koenzym B), którego brakuje do utworzenia cząsteczki metanu
dokładnie w miejsce, gdzie we właściwym enzymie znajduje się atom niklu. Katalizuje on jej połączenie z ostatnim atomem wodoru (dostarczanym przez koenzym B), którego brakuje do utworzenia cząsteczki metanu 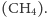
Nad tym, w jaki sposób to połączenie się dokonuje, zastanawiano się od kilkudziesięciu lat. Wyglądało na to, że reakcja zachodzi zbyt szybko, żeby można było rozpoznać, jaką drogą zachodzi.
Dominował pogląd, że na moment grupa metylowa jest dołączana do atomu niklu. Według alternatywnej koncepcji koenzym M zamiast dostarczyć atomowi niklu grupę metylową, dokuje drugim końcem (tym sulfonowym: 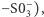 uwalniając rodnik metylowy, który już bezpośrednio odbiera atom wodoru od koenzymu B. Ta druga możliwość była mniej popularna, bo rodnik metylowy potrafi narobić niezłego bałaganu, szukając partnera dla swojego niesparowanego elektronu - wydawało się, że natura nie poszła na aż taki hazard.
uwalniając rodnik metylowy, który już bezpośrednio odbiera atom wodoru od koenzymu B. Ta druga możliwość była mniej popularna, bo rodnik metylowy potrafi narobić niezłego bałaganu, szukając partnera dla swojego niesparowanego elektronu - wydawało się, że natura nie poszła na aż taki hazard.
W ostatnio opublikowanej pracy [1] udało się to sprawdzić. Po pierwsze, spowolniono reakcję o trzy rzędy wielkości. Następnie, za pomocą spektroskopii elektronowego rezonansu paramagnetycznego sprawdzono, że pośredni stan Ni(III) połączonego z grupą metylową nie występuje. Natomiast za pomocą magnetycznego dichroizmu kołowego udało się stwierdzić występowanie połączenia Ni(II) z koenzymem M, co ostatecznie przesądziło o wykorzystywaniu przez naturę rodnika metylowego w omawianej reakcji.
Reakcja z rodnikiem metylowym w stanie przejściowym została również wymodelowana komputerowo. Okazało się, że jest ona bardzo opłacalna energetycznie.
Ponieważ reakcja ta nie powoduje dewastacji archeonu, to znaczy, że zachodzi niezwykle precyzyjnie. Żarłoczny rodnik musi od razu trafić na właściwą ofiarę - koenzym B.
Ponieważ omawiana reakcja katalityczna może zachodzić w obie strony, to zrozumienie stojącego za nią mechanizmu otwiera drogę do poszukiwania efektywnych schematów przeobrażania metanu.