Masy atomowe pierwiastków występujących naturalnie w przyrodzie wypełniają przedział od 1 (wodór) do 244 (pluton), a promienie atomowe, przedział od 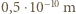 (wodór) do
(wodór) do 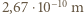 (cez) - wynik oszacowania zależy od charakteru wiązań, jakie atom tworzy, gdy wchodzi w związki chemiczne. Masy atomów nie zależą od tworzonych przez nie wiązań, a więc w obliczeniach posłużymy się ich masami. Spróbujmy oszacować "typową" masę atomów wchodzących w skład Ziemi. W atmosferze mamy niemal wyłącznie azot i tlen o masach atomowych 14 i 16,w skorupie Ziemi dominuje tlen oraz krzem o masie atomowej 28, a jądro Ziemi składa się głównie z żelaza i niklu o masach atomowych 56 i 59. Przyjmijmy, że typowa liczba masowa to 50, i obliczmy, ile takich atomów "składa" się na masę Ziemi:
(cez) - wynik oszacowania zależy od charakteru wiązań, jakie atom tworzy, gdy wchodzi w związki chemiczne. Masy atomów nie zależą od tworzonych przez nie wiązań, a więc w obliczeniach posłużymy się ich masami. Spróbujmy oszacować "typową" masę atomów wchodzących w skład Ziemi. W atmosferze mamy niemal wyłącznie azot i tlen o masach atomowych 14 i 16,w skorupie Ziemi dominuje tlen oraz krzem o masie atomowej 28, a jądro Ziemi składa się głównie z żelaza i niklu o masach atomowych 56 i 59. Przyjmijmy, że typowa liczba masowa to 50, i obliczmy, ile takich atomów "składa" się na masę Ziemi:
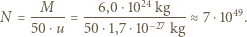
Dla "sprawdzenia" oszacujmy, ile "typowych atomów" wypełni objętość Ziemi. Promienie atomów najczęściej występujących na Ziemi mieszczą się w przedziale od 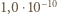 m do
m do 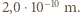 Przyjmijmy promień "typowego" atomu
Przyjmijmy promień "typowego" atomu 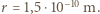 Otrzymujemy, że do "wypełnienia" objętości Ziemi potrzeba:
Otrzymujemy, że do "wypełnienia" objętości Ziemi potrzeba:
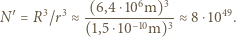
Przyjęliśmy kulisty kształt atomów i pominęliśmy fakt, że ciasno upakowane kule wypełniają "tylko" około 3/4 objętości przestrzeni, oraz wpływ ogromnych ciśnień we wnętrzu Ziemi (do około 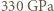 ). Zgodność otrzymanych wartości
). Zgodność otrzymanych wartości 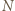 i
i 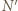 jest nawet nieco zaskakująca.
jest nawet nieco zaskakująca.
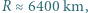 masa Ziemi
masa Ziemi 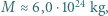 jednostka masy atomowej (
jednostka masy atomowej ( 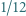 masy atomu
masy atomu 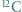 )
) 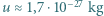 Pozostałe informacje znajdź, analizując dane przytaczane w układzie okresowym pierwiastków.
Pozostałe informacje znajdź, analizując dane przytaczane w układzie okresowym pierwiastków.
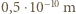 (wodór) do
(wodór) do 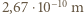 (cez) - wynik oszacowania zależy od charakteru wiązań, jakie atom tworzy, gdy wchodzi w związki chemiczne. Masy atomów nie zależą od tworzonych przez nie wiązań, a więc w obliczeniach posłużymy się ich masami. Spróbujmy oszacować "typową" masę atomów wchodzących w skład Ziemi. W atmosferze mamy niemal wyłącznie azot i tlen o masach atomowych 14 i 16,w skorupie Ziemi dominuje tlen oraz krzem o masie atomowej 28, a jądro Ziemi składa się głównie z żelaza i niklu o masach atomowych 56 i 59. Przyjmijmy, że typowa liczba masowa to 50, i obliczmy, ile takich atomów "składa" się na masę Ziemi:
(cez) - wynik oszacowania zależy od charakteru wiązań, jakie atom tworzy, gdy wchodzi w związki chemiczne. Masy atomów nie zależą od tworzonych przez nie wiązań, a więc w obliczeniach posłużymy się ich masami. Spróbujmy oszacować "typową" masę atomów wchodzących w skład Ziemi. W atmosferze mamy niemal wyłącznie azot i tlen o masach atomowych 14 i 16,w skorupie Ziemi dominuje tlen oraz krzem o masie atomowej 28, a jądro Ziemi składa się głównie z żelaza i niklu o masach atomowych 56 i 59. Przyjmijmy, że typowa liczba masowa to 50, i obliczmy, ile takich atomów "składa" się na masę Ziemi: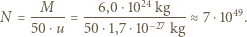
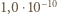 m do
m do 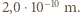 Przyjmijmy promień "typowego" atomu
Przyjmijmy promień "typowego" atomu 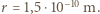 Otrzymujemy, że do "wypełnienia" objętości Ziemi potrzeba:
Otrzymujemy, że do "wypełnienia" objętości Ziemi potrzeba: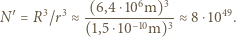
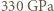 ). Zgodność otrzymanych wartości
). Zgodność otrzymanych wartości 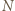 i
i 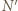 jest nawet nieco zaskakująca.
jest nawet nieco zaskakująca.